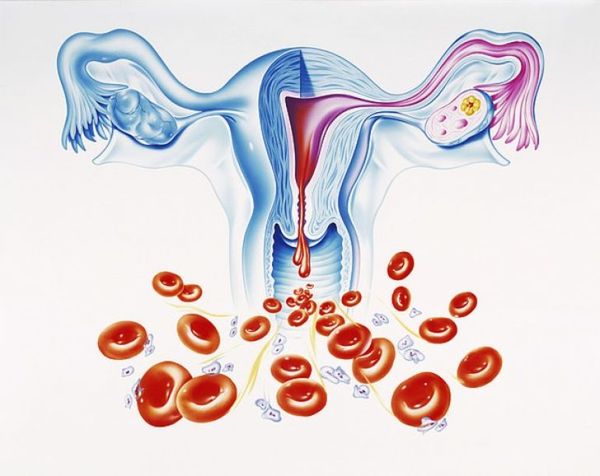
Микроскопический полиангиит (МПА, Microscopic polyangiitis) — это воспаление мелких сосудов (капиляров, венул и артериол) в разных органах, которое протекает с отмиранием (некрозом) клеток сосудистой стенки.
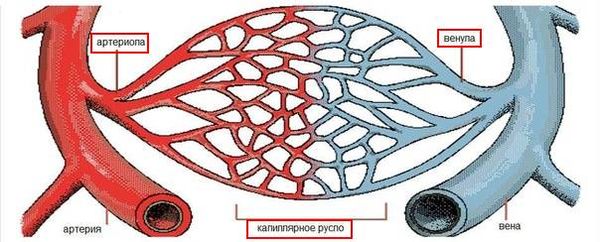
Сосуды, которые поражаются при МПА
Чаще всего МПА поражает сосуды почек и лёгких. Поражение почек протекает в виде некротизирующего гломерулонефрита. При этой болезни воспаляются и отмирают стенки капилляров почечных клубочков (гломерул), которые фильтруют кровь. Такое состояние может проявляться отёками ног, уменьшением объёма мочи и изменением её цвета. По мере прогрессирования болезни могут поражаться все клубочки с тотальным некрозом капиллярных петель, что быстро приводит к распространённому нефросклерозу (рубцеванию) и терминальной почечной недостаточности, когда требуется диализ или пересадка почки.
В лёгких при МПА обычно развивается альвеолярный капиллярит (воспаление капилляров) или фиброз, что проявляется одышкой и кровохарканьем .
Термин «микроскопический полиартериит» впервые упомянул в литературе в 1948 году Davson J., когда описывал сочетание генерализованного (распространённого) поражения мелких и средних сосудов и быстропрогрессирующего гломерулонефрита .
Распространённость
Точная распространённость МПА неизвестна. По некоторым сведениям, она составляет около 6,8 случаев на 1 млн населения. По другим данным, частота МПА составляет приблизительно 1,5 случая на 100 тыс. человек, а среди детей –– 2,4–2,75 нa 1 млн .
Микроскопический полиангиит обычно развивается в среднем возрасте. Немного чаще диагностируется у мужчин: соотношение от 1:1 до 1,8:1 .
Причины
Болезнь относится к АНЦА-ассоциированным васкулитам. Термином «васкулит» обозначают воспаление сосудов, а «АНЦА-ассоциированный» означает, что в крови пациентов выявляются антитела к цитоплазме нейтрофилов, их ещё называют антинейтрофильными цитоплазматическими антителами (АНЦА). Именно с ними связывают развитие МПА.
АНЦА — это белки, направленные против различных компонентов нейтрофилов (клеток крови, которые обеспечивают иммунную защиту). При МПА вырабатываются АНЦА к миелопероксидазе (МПО) и протеиназе-3 (Пр3) — это ферменты, которые находятся в гранулах нейтрофилов и усиливают его антимикробное действие.
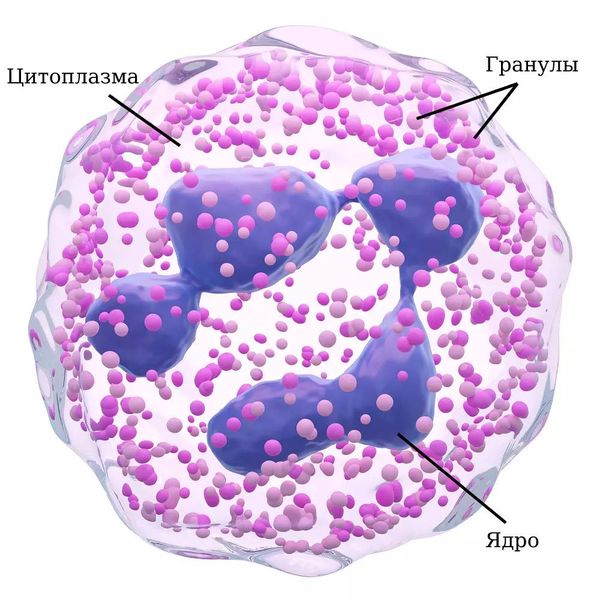
Нейтрофил
В норме антитела должны работать только против «чужеродных» агентов. Но в некоторых случаях иммунная система становится сверхактивной и начинает вырабатывать антитела против клеток собственного организма, например против компонентов нейтрофилов, как при МПА. Причины такой сверхактивности иммунитета неизвестны.
Однако АНЦА выявляются не у всех пациентов с МПА: на момент постановки диагноза они обнаруживаются только в 70 % случаев, а в большинстве случаев ограниченного МПА вообще не обнаруживаются . Это привело к пониманию, что в развитии болезни могут играть роль и другие факторы:
- Инфекции. Предположить этот фактор позволило то, что проявления разных инфекционных процессов и МПА совпадают.
- Лекарства: Гидралазин, тионамиды, Сульфасалазин и Миноциклин.
- Генетические факторы. Согласно исследованию, проведённому в Европе, в развитии АНЦА-ассоциированных васкулитов участвуют такие гены, как HLA-DP, HLA-DR3 и альфа-1-антитрипсин .
MПA также может быть связан с воздействием кремнезёма (например, кремниевой пыли при производстве стекла), вызывая аутоиммунитет у пациентов с некоторой генетической предрасположенностью .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы микроскопического полиангиита
Для МПА характерно поражение нескольких органов, быстропрогрессирующее течение (когда симптомы развиваются в течение нескольких дней или недель) и высокая смертность . Но возможно и вялотекущее течение, когда неспецифические симптомы, такие как лихорадка или боли в суставах (артралгия), могут присутствовать в течение нескольких месяцев или лет до постановки диагноза.
Обычно в начале болезни возникают общие симптомы: лихорадка, боли в суставах и мышцах (миалгия), снижение веса.
Затем присоединяются другие проявления:
- нарушение мочеиспускания;
- кашель с кровохарканьем или без него;
- пальпируемая пурпура на коже (красные или фиолетовые пятна, которые можно ощутить при прощупывании);
- множественный мононеврит — одновременное поражение двух или более периферических нервов в разных частях тела, что проявляется болью, онемением, слабостью и потерей контроля над мышцами в зоне поражённых нервов;
- судороги и другие неспецифические неврологические жалобы;
- боль в животе;
- желудочно-кишечное кровотечение;
- боль в груди, в глазах и яичках;
- синусит (насморк, заложенность носа).
У некоторых пациентов заболевание начинается резко и развивается очень быстро: возникает выраженное кровохарканье, появляется кровь в моче (гематурия) или развивается почечная недостаточность .
Примерно у трети больных в начале болезни могут быть изменения верхних дыхательных путей в виде атрофии слизистой носа и некротического ринита. Но эти изменения обратимы, не сопровождаются разрушением ткани и не приводят к деформации носа .
Почки
Согласно результатам исследований, от 80 до 100 % пациентов с МПА имеют почечные проявления: от бессимптомного мочевого осадка до терминальной стадии почечной недостаточности .
Основным почечным признаком МПА является быстропрогрессирующий гломерулонефрит (БПГН) . При этом сначала беспокоят общие симптомы, такие как слабость, лихорадка, боли в суставах и другие, затем появляются периферические отёки (как правило, отекают ноги и лицо), уменьшается объём отделяемой мочи и изменяется её цвет — моча становится красноватой и мутной .
Лёгкие
По одним данным, лёгкие при МПА поражаются в 25–55 % случаев . Но в другом исследовании, где оценивалось состояние 40 пациентов с МПА за 10 лет, симптомы поражения лёгких наблюдались у 80 % пациентов, а рентгенологические изменения были обнаружены у 92 % .
Чаще всего при поражении лёгких возникает диффузное альвеолярное кровотечение, которое проявляется кровохарканьем, кашлем и болью в груди. Но у некоторых пациентов может развиться хронический интерстициальный фиброз, при этом лёгочная ткань заменится на грубую рубцовую, что со временем приведёт к дыхательной недостаточности с одышкой, тахикардией, цианозом (синюшностью кожи) и другими проявлениями .
Кожа
Поражения кожи наблюдаются у 30–60 % пациентов и являются начальным признаком МПА у 15–30 % пациентов . Кожные проявления включают пальпируемую пурпуру, сетчатое ливедо (пятнистый сетчатый сосудистый рисунок), узелки и кожные язвы с некрозом, также могут возникать инфаркты (прекращение кровоснабжения) ногтевого ложа (проявляется пурпурными или чёрными полосами, точками или пятнами под ногтем), иногда возникает ишемия пальцев, т. е. нарушается их кровоснабжение, что проявляется болью, онемением, покраснением, бледностью или синюшностью кожи. Кожные симптомы могут быть связаны с болями в суставах у пациентов с МПА .
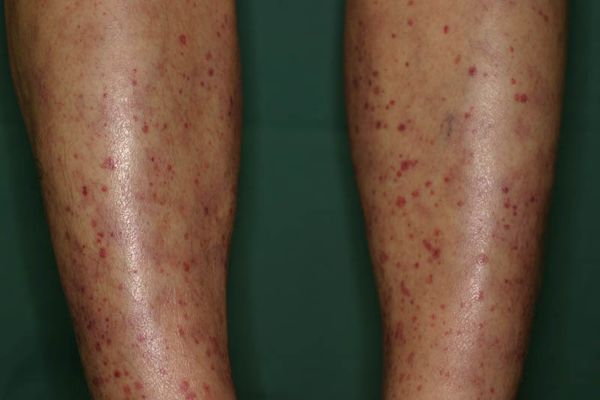
Проявления МПА на коже [29]
Желудочно-кишечный тракт
Наиболее частым симптомом поражения желудочно-кишечного тракта при МПА является боль в животе. Также могут наблюдаться тошнота, рвота, диарея, кровь в кале. В некоторых случаях возникает желудочно-кишечное кровотечение, хотя массивное кровотечение встречается редко .
Нервная система
Как правило, вовлекается периферическая нервная система. При поражении нервов возникает слабость мышц, потеря чувствительности (онемение), покалывания и боль в руках или ногах.
Редко поражается центральная нервная система, в таких случаях может наблюдаться синдром задней обратимой энцефалопатии (обратимого поражения мозга из-за отёка), при котором возможны судороги, нарушение сознания, головные боли и зрительные нарушения. Проявления со стороны центральной нервной системы также могут включать кровоизлияние в мозг и инфаркты головного мозга, всё это связано с воспалением сосудов головного мозга .
Глаза
У 30 % пациентов с МПА развивается склерит и эписклерит — воспаление склеры (белков глаз) и соединительной ткани между склерой и конъюнктивой, что сопровождается болью и покраснением глаз .
Сердце
Сердце поражается редко, однако может беспокоить гипертония и признаки сердечной недостаточности (например, одышка, учащённое сердцебиение, отёки). Иногда развивается инфаркт миокарда и перикардит .
Суставы
При МПА поражения суставов встречаются примерно у 38–65 % больных . В половине случаев наблюдают признаки артрита (воспаления) крупных суставов, который проявляется болью в суставах, отёчностью и ограничением подвижности . В некоторых случаях эти симптомы бывают первыми проявлением МПА.
Патогенез микроскопического полиангиита
Точный механизм развития микроскопического полиангиита неизвестен. Предполагается, что АНЦА к ферментам МПО и Пр3 образуются под воздействием разных предрасполагающих генетических, экологических и других факторов и находятся в организме, пока не появится какой-либо триггер, например инфекция .
Дальше в развитии болезни выделяют два этапа:
- На первом этапе в ответ на инфекцию иммунные и некоторые другие клетки вырабатывают провоспалительные цитокины — специальные вещества, которые запускают воспаление. Эти цитокины воздействуют на нейтрофилы, в результате чего МПО и Пр3 перемещаются из гранул нейтрофила к его поверхности . Так нейтрофилы готовятся к активации, т. е. к борьбе с чужеродными агентами, попавшими в организм.
- На втором этапе АНЦА связываются с МПО или Пр3 на поверхности нейтрофила, что приводит к его активации. Активированные нейтрофилы связываются с эндотелием (внутренним слоем) сосудов. Происходит дегрануляция нейтрофилов — из гранул высвобождаются активные формы кислорода и протеазы, которые повреждают внутреннюю стенку сосудов, вызывая её воспаление . Отложение МПО и Пр3 в тканях приводят к привлечению T-клеток и моноцитов, усиливая повреждение ткани.
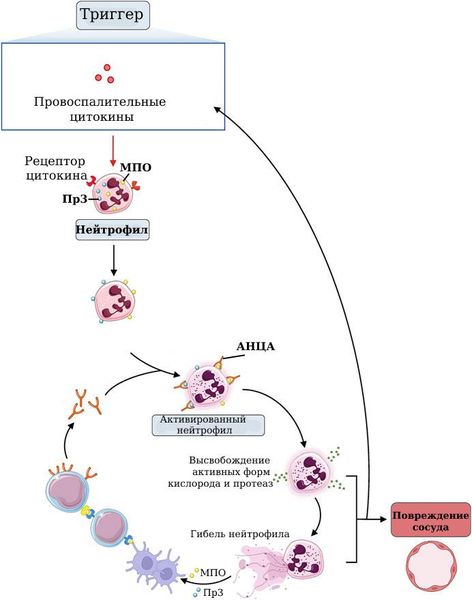
Механизм развития микроскопического полиангиита [31]
При поражении эндотелия возможна утечка сывороточных белков и факторов свёртывания, что вызывает некроз сосудистой стенки и тромбоз . Из-за этого ограничивается приток крови к органам и тканям, что может вызывать различные симптомы, такие как боли, отёки, кровоизлияния и нарушение работы почек и лёгких.
Классификация и стадии развития микроскопического полиангиита
Микроскопический полиангиит относится к АНЦА-ассоциированным васкулитам. Кроме него, к этой группе относят:
- гранулематоз с полиангиитом (гранулематоз Вегенера);
- эозинофильный гранулематоз с полиангиитом (синдром Чёрджа — Стросса).
АНЦА-ассоциированный васкулит — это, в свою очередь, один из системных васкулитов. Термин «системный» означает, что болезнь затрагивает несколько органов и систем.
Различают несколько вариантов клинического течения МПА:
- молниеносный — летальный исход наступает в течение нескольких недель из-за лёгочного кровотечения или острой почечной недостаточности;
- подострый — характерен тяжёлый нефротический синдром или быстропрогрессирующий гломерулонефрит;
- непрерывно рецидивирующий — обострения наступают каждые 6–12 месяцев, преобладает неспецифическая симптоматика, гломерулонефрит, кровохарканье;
- латентный — доминируют суставной синдром (боли, отёки, ограничение движений в суставах), гематурия, кровохарканье.
Диагностические критерии 1990 года:
- Лихорадка, недомогание, похудание, боли в мышцах.
- Артрит, боли в суставах.
- Поражение лёгких.
- Быстропрогрессирующий гломерулонефрит.
- Кожные проявления.
- Желудочно-кишечные проявления.
- Поражение нервной системы.
Для постановки диагноза необходимо наличие 4-го критерия и трёх любых .
Стадии МПА:
- В активной фазе воспаление сосудов наиболее выражено. Пациенты могут испытывать сильные симптомы, такие как лихорадка, боль в суставах, общая усталость, в крови при этом может повышаться уровень АНЦА. Эта фаза может привести к повреждению сосудов и органов.
- Во время ремиссии воспаление утихает, симптомы уменьшаются или исчезают, поэтому пациенты чувствуют себя лучше. Уровень АНЦА в крови может уменьшиться.
Стадии МПА могут переходить друг в друга в зависимости от активности заболевания и эффективности лечения.
Осложнения микроскопического полиангиита
Без лечения МПА может привести к необратимому повреждению органов. Осложнения МПА будут зависеть от конкретной поражённой системы органов.
Почечная недостаточность. Наиболее частым осложнением МПА является прогрессирующая почечная недостаточность, вплоть до терминальной стадии, при которой требуется диализ или пересадка почки.
При терминальной стадии состояние очень тяжёлое. Выделение мочи сильно снижается, вплоть до полного её отсутствия. Характерна сильная слабость, зябкость и апатия. Резко снижается аппетит, иногда пациенты полностью отказываются от пищи из-за частой тошноты и отвращения к еде. Кожа бледная, сухая, желтушная, с серым оттенком. Могут возникать мышечные судороги .
Прогрессирующая почечная недостаточность — это один из главных неблагоприятных факторов, влияющих на продолжительность и качество жизни пациентов с МПА, наряду с поражением лёгких .
Венозные тромбоэмболические осложнения. У больных с АНЦА-ассоциированными васкулитами, в том числе МПА, могут развиваться венозные тромбоэмболические осложнения. К ним относятся тромбоз глубоких вен и тромбоэмболия лёгочной артерии. По данным исследований, венозные тромбоэмболические осложнения чаще выявлялись у мужчин и были связаны с поражением лёгких в рамках системного васкулита .
Тромбоэмболия лёгочной артерии
Сердечно-сосудистые осложнения. Исследования показали, что у пациентов пожилого возраста с высоким нижним артериальным давлением (больше 90 мм рт. ст.) при нормальном верхнем давлении и наличием Пр3-АНЦА чаще развиваются сердечно-сосудистые болезни, например инфаркт миокарда и перикардит .
Диагностика микроскопического полиангиита
МПА является одним из труднодиагностируемых системных васкулитов, так как его проявления могут быть весьма разнообразными: от кожной сыпи до молниеносного мультисистемного поражения. Поэтому для постановки диагноза необходим очень тщательный и системный подход. Обследование пациента с подозрением на МПА должно включать сбор жалоб и анамнеза (истории жизни и болезни), осмотр, лабораторное, инструментальное и гистопатологическое обследование.
Сбор жалоб и анамнеза
Диагностикой и лечением микроскопического полиангиита занимается ревматолог. Но на начальном этапе болезни, когда беспокоит только незначительное недомогание, лихорадка, кожная сыпь или боли в суставах, пациенты довольно часто обследуются у узких специалистов: дерматолога, отоларинголога, офтальмолога, пульмонолога, фтизиатра, нефролога и др. Но причину беспокойства часто не находят. Врач-ревматолог при сборе анамнеза обратит внимание на этот факт.
В целом при подозрении на системное заболевание врач уточнит у пациента:
- где он работает, так как MПA может быть связан с воздействием кремниевой пыли;
- какие препараты пациент принимает или принимал;
- какие заболевания есть у близких родственников.
Лабораторная диагностика
Лабораторная оценка включает анализы крови и мочи.
1. Анализы крови:
- Рутинный общий анализ крови. Можно обнаружить лейкоцитоз (повышенный уровень лейкоцитов), анемию и повышенную скорость оседания эритроцитов (СОЭ).
- Анализы на электролиты (калий, натрий, хлориды, кальций, фосфор). Изменения их уровня могут указывать на почечную недостаточность.
- Анализ на уровни азота мочевины и креатинина. Их повышение может указывать на нарушение функции почек.
- Посев крови. Позволяет исключить бактериальный эндокардит.
- Анализ крови на уровень компонентов системы комплемента С3 и С4. Они обычно в норме.
В основе лабораторного подтверждения диагноза лежит обнаружение в крови АНЦА к МПО и Пр3. Тест на АНЦА положительный в 80 % случаев, среди них МПО-АНЦА присутствуют в 60 %, тогда как Пр3-АНЦА присутствуют в 40 % .
2. Анализ мочи. Выявление в моче эритроцитов, белка и лейкоцитов (гематурия, протеинурия и лейкоцитурия), а также зернистых или эритроцитарных цилиндров укажут на поражение почек.
Инструментальная диагностика
Рентгенография и компьютерная томография (КТ) грудной клетки выполняются, чтобы оценить поражения лёгких у пациентов с кровохарканьем. По результатам может обнаруживаться лёгочное кровотечение и/или фиброз. Эти исследования также помогают дифференцировать (отличить) МПА от другого АНЦА-ассоциированного васкулита — гранулематоза с полиангиитом (ГПА): для ГПА характерны полостные и узловатые поражения, которых нет при МПА.
Компьютерная томография брюшной полости может проводиться, чтобы исключить острый панкреатит, так как при МПА иногда возникает боль в животе, как при панкреатите, но на самом деле это может быть проявлением ишемического энтероколита.
Мезентериальная ангиография (исследование кровеносных сосудов, питающих тонкий и толстый кишечник). Может использоваться, чтобы исключить узелковый полиартериит, при котором чаще поражаются средние сосуды .
Электрокардиография (ЭКГ). Проводится при подозрении на инфаркт миокарда, перикардит или сердечную недостаточность.
Электрокардиография
Гастроинтестинальная эндоскопия. Выполняется при желудочно-кишечных кровотечениях.
Электромиография (ЭМГ). Это исследование нервной проводимости, оно может выполняться, если есть признаки поражения нервов (слабость мышц, онемение, покалывания). В таких случаях ЭМГ показывает острую аксонопатию — поражение аксонов, которые проводят сигналы вдоль нервов.
Гистопатологическая диагностика
Чтобы подтвердить диагноз, по возможности проводится биопсия кожи, почек и лёгких для поиска признаков васкулита и иммунных отложений.
Признаки МПА при гистопатологическом исследовании:
- Фибриноидный некроз капилляров и артериол клубочка. При фибриноидном некрозе клетки капилляров и артериол погибают (происходит их некроз) и особый белок крови (фибрин) просачивается из крови и окружает повреждённую ткань.
- Полулуния в клубочках (скопление плазменных белков и воспалительных клеток в полости капсулы Шумлянского — Боумена в форме полулуния).
- Иммунные депозиты (скопления иммунных комплексов) в ткани почки отсутствуют .
Степень воспаления, которая определяется при биопсии почки, позволяет измерить активность заболевания и выбрать подходящее лечение.
Лечение микроскопического полиангиита
Если установлен диагноз «микроскопический полиангиит», следует избегать физических и психоэмоциональных перегрузок и переохлаждения, не принимать лекарства и не использовать средства нетрадиционной медицины без назначения врача.
Основой питания при васкулитах является исключение аллергенов: цитрусовых, яиц, усилителей вкуса, мёда, грибов, промышленных консервантов и др. Также следует отказаться от жареных и жирных блюд, ввести в рацион большое количество свежих фруктов и овощей, обязательно употреблять кисломолочные продукты и крупы.
Лечение МПА предполагает различные комбинации глюкокортикоидов (например, Преднизолона) и других иммунодепрессантов: Циклофосфамида, Ритуксимаба, Метотрексата, Азатиоприна и генно-инженерных биологических препаратов. Выбор препарата будет зависеть от распространённости заболевания, скорости прогрессирования и степени воспаления.
При активном МПА первая цель лечения — достичь ремиссии, вторая — поддерживать её.
Лечение, направленное на достижение ремиссии
Как правило, ремиссия достигается с помощью комбинации глюкокортикоидов и Циклофосфамида. Это метод первой линии при тяжёлой форме заболевания. В некоторых случаях, например если есть побочные эффекты, вместо Циклофосфамида могут использовать Ритуксимаб . Дозы и длительность курса определяет лечащий врач. Как правило, ремиссия наступает через 2–6 месяцев. В ходе такого лечения врач будет контролировать показатели общего анализа крови, чтобы не допустить слишком сильного снижения уровня лейкоцитов, в частности нейтрофилов.
При тяжёлой форме болезни, например в случае опасного для жизни лёгочного кровотечения или при тяжёлой почечной недостаточности, в дополнение к глюкокортикоидам и Циклофосфамиду могут назначить плазмаферез (очистку крови). Этот дополнительный метод помогает улучшить функцию почек и снизить риск терминальной почечной недостаточности .
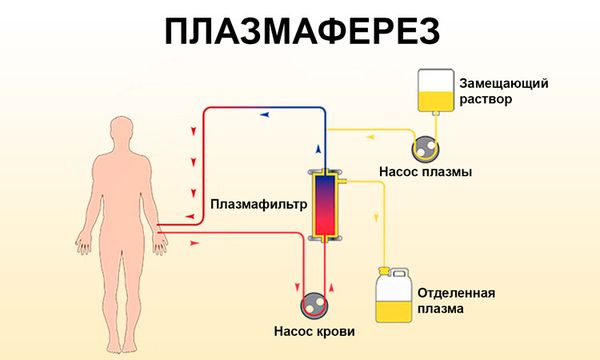
Плазмаферез
Лечение рецидива МПА такое же, как и для достижения ремиссии. Для лечения рефрактерных заболеваний (т. е. плохо поддающихся лечению) может использоваться внутривенный иммуноглобулин.
Лечение, направленное на поддержание ремиссии
После полной ремиссии приступают к поддерживающей терапии. Ремиссию поддерживают одним из следующих препаратов: Циклофосфамид, Азатиоприн, Преднизолон, Циклоспорин, Ритуксимаб или Метотрексат .
Пациентам с ВИЧ-инфекцией или высоким риском пневмонии врач может назначить низкие дозы комбинированного противомикробного препарата, содержащего сульфаметоксазол и триметоприм для профилактики пневмоцистной пневмонии . Частота профилактики зависит от эпидемиологической обстановки.
Осложнения лечения
Препараты, которыми лечат МПА, могут вызывать побочные эффекты. Например, есть данные, что при приёме Циклофосфамида повышается риск рака мочевого пузыря. Глюкокортикоиды вызывают потерю костной массы, гипергликемию (повышение уровня глюкозы в крови), мышечную слабость и проблемы с кожей .
Прогноз. Профилактика
При соответствующем лечении состояние улучшается примерно у 90 % пациентов, а примерно 75 % достигают полной ремиссии. 5-летняя выживаемость составляет 75 %, это значит, что через 5 лет после постановки диагноза 75 % пациентов остаются живы .
Однако при МПА выживаемость всё же ниже, чем при синдроме Чёрджа — Стросса или гранулематозе с полиангиитом. Вероятно, это связано с почечной недостаточностью, присутствующей в начале заболевания . По данным одного исследования, пациенты с поражением лёгких имели более высокий риск развития поражения почек и сердечно-сосудистой системы и были более склонны к развитию лёгочного фиброза .
Причиной смерти при МПА являются массивные лёгочные кровотечения, инфекционные осложнения, связанные с проводимой терапией, а также острая дыхательная и почечная недостаточность.
Специфических мер профилактики, т. е. вакцин, против васкулитов не существует. Чтобы снизить риск их развития, рекомендуется:
- Отказаться от курения, в том числе пассивного.
- Исключить длительные стрессы.
- Регулярно лечить очаги хронической инфекции.
- Строго придерживаться режима отдыха и работы.
- Не допускать длительного переохлаждения и перегрева, а также воздействия аллергенов и агрессивных химических веществ.
- Питаться разнообразной, здоровой и качественной пищей.
- Предупреждать дефицит витамина D.
- Сделать вакцину против гриппа и COVID-19.
Список литературы
- Hashmi M. F., Jain V., Tiwari V. Microscopic Polyangiitis // StatPearls Publishing. — 2023.ссылка
- Wainwright J., Davson J. The renal appearances in the microscopic form of periarteritis nodosa // J Pathol Bacteriol.— 1950. — Vol. 62, № 2. — Р. 189–196.ссылка
- Мухин Н. А., Семенкова Е. Н., Кривошеев О. Г., Новиков П. И. Применение ритуксимаба при тяжёлых АНЦА-ассоциированных системных васкулитах // Клиническая нефрология. — 2010.— № 2. — С. 40–45.
- Насонова В. А., Насонов Е. Л. Рациональная фармакотерапия ревматических заболеваний. — М.: Литтерра, 2003. — С. 506.
- Berti A., Cornec D., Crowson C. S. et al. The Epidemiology of Antineutrophil Cytoplasmic Autoantibody-Associated Vasculitis in Olmsted County, Minnesota: A Twenty-Year US Population-Based Study // Arthritis & rheumatology. — 2017. — Vol. 69, № 12. — Р. 2338–2350.ссылка
- Vamvakopoulos J., Savage C., Наrper L. ANCA-associated vasculitides in children — lessons from the adult literature // Pediatr Nephrol. — 2010. — Vol. 25, № 8. — Р. 1397–1407.ссылка
- de Lind van Wijngaarden R. A., van Rijn L., Hagen E. C. et al. Hypotheses on the etiology of antineutrophil cytoplasmic autoantibody associated vasculitis: the cause is hidden, but the result is known // Clin J Am Soc Nephrol. — 2008. — Vol. 3, № 1. — Р. 237–252. ссылка
- Chung S. A., Seo P. Microscopic polyangiitis // Rheum Dis Clin North Am. — 2010. — Vol. 36, № 3. — Р. 545–558.ссылка
- Eriksson P., Segelmark M., Hallböök O. Frequency, Diagnosis, Treatment, and Outcome of Gastrointestinal Disease in Granulomatosis with Polyangiitis and Microscopic Polyangiitis // J Rheumatol. — 2018. — Vol. 45, № 4. — Р. 529–537.ссылка
- Wang H., Sun L., Tan W. Clinical features of children with pulmonary microscopic polyangiitis: report of 9 cases // PLoS One. — 2015. — Vol. 10, № 4.ссылка
- Wilke L., Prince-Fiocco M., Fiocco G. P. Microscopic polyangiitis: a large single-center series // J Clin Rheumatol. — 2014. — Vol. 20, № 4. — Р. 179–182. ссылка
- Karras A. Microscopic Polyangiitis: New Insights into Pathogenesis, Clinical Features and Therapy // Semin Respir Crit Care Med. — 2018. — Vol. 39, № 4. — Р. 459–464. ссылка
- Муркамилов И. Т. и др. Микроскопический полиангиит: диагностические и терапевтические подходы к лечению (обзор литературы и описание клинического случая) // Научное наследие. — 2020. — № 48. — С. 26–33.
- Massicotte-Azarniouch D., Herrera C. A., Jennette J. C. et al. Mechanisms of vascular damage in ANCA vasculitis // Semin Immunopathol. — 2022. — № 44, № 3. — Р. 325–345. ссылка
- Kitching A. R., Anders H. J., Basu N. et al. ANCA-associated vasculitis // Nat Rev Dis Primers. — 2020. — Vol. 6, № 1. — Р. 71.ссылка
- Robson J., Doll H., Suppiah R. et al. Glucocorticoid treatment and damage in the anti-neutrophil cytoplasm antibody-associated vasculitides: long-term data from the European Vasculitis Study Group trials // Rheumatology (Oxford). — 2015. — Vol. 54, № 3. — Р. 471–481.ссылка
- Hassan T. M., Hassan A. S., Igoe A. et al. Lung involvement at presentation predicts disease activity and permanent organ damage at 6, 12 and 24 months follow — up in ANCA — associated vasculitis // BMC Immunol. — 2014. — Vol. 15. ссылка
- Specks U., Merkel P. A., Seo P., Spiera R. et al. Efficacy of remission-induction regimens for ANCA-associated vasculitis // N Engl J Med. — 2013. — Vol. 369, № 5. — Р. 417–427. ссылка
- Jayne D., Rasmussen N., Andrassy K. et al. A randomized trial of maintenance therapy for vasculitis associated with antineutrophil cytoplasmic autoantibodies // N Engl J Med. — 2003. — Vol. 349, № 1. — Р. 36–44. ссылка
- Iida T., Adachi T., Tabeya T. et al. Rare type of pancreatitis as the first presentation of anti-neutrophil cytoplasmic antibody-related vasculitis // World J Gastroenterol. — 2016. — Vol. 22, № 7. — Р. 2383–2390. ссылка
- Макаров Е. А., Новиков П. И., Шевцова Т. П. и др. Венозные тромбоэмболические осложнения при АНЦА-ассоциированных васкулитах // Клиническая фармакология и терапия. — 2017. — № 3. — С. 37–42.
- Уткина Е. И., Мясоедова С. Е., Манохин В. Ю. и др. Микроскопический полиангиит: особенности течения и трудности диагностики (клиническое наблюдение) // РМЖ. Медицинское обозрение. — 2018. — № 1 (II). — С. 118–120.
- Смирнова И. Г., Буланов Н. М., Зыкова А. С. и др. Серопозитивный и серонегативный варианты гранулематоза с полиангиитом: влияние АНЦА на клиническую картину и прогноз заболевания // Клиническая фармакология и терапия. — 2020. — № 1. — С. 36–40.
- Frankel S. K., Schwarz M. I. The pulmonary vasculitides // Am J Respir Crit Care Med. — 2012. — Vol. 186, № 3. — Р. 216–224. ссылка
- Ревматология: национальное руководство / под ред. Е. Л. Насонова, В. А. Насоновой. — М.: ГЭОТАР-Медиа, 2010. — С. 552.
- Зборовская И. А. и др. Учебник практической ревматологии: руководство для врачей. — Ростов-н/Д, 2016. — С. 198.
- Lyons P. A., Rayner T. F., Trivedi S. et al. Genetically Distinct Subsets within ANCA-Associated Vasculitis // N Engl J Med. — 2012. — Vol. 367, № 3. — Р. 214–223.ссылка
- Николаев А. Ю. Хроническая почечная недостаточность: клиника, диагностика и лечение // РМЖ. — 2000. — № 3. — С. 138.
- Kawakami T. Microscopic Polyangiitis // CancerTherapyAdvisor. — 2017.
- Falk R. J., Jennette J. C. ANCA Are Pathogenic — Oh Yes They Are! // Journal of the American Society of Nephrology. — 2002. — Vol. 13, № 7. — Р. 1977–1979.
- Ge S., Zhu X., Xu Q. et al. Neutrophils in ANCA-associated vasculitis: Mechanisms and implications for management // Front Pharmacol. — 2022. — Vol. 13.ссылка
- Классификации заболеваний внутренних органов и структурирование клинического диагноза: методическое пособие. — Ростов-н/Д: РостГМУ, 2009. — 115 с.
- Jayne D. Update on the European Vasculitis Study Group trials // Curr Opin Rheumatol. — 2001. — Vol. 13, № 1. — Р. 48–55.ссылка
Современные методы исследования и лечения
Микроскопический полиангиит (МПА) требует комплексного подхода, охватывающего широкий спектр диагностических методик и терапевтических вмешательств. Важно не только правильно поставить диагноз, но и подобрать наиболее эффективное и персонализированное лечение для каждого пациента.
Методы исследования
Для диагностики МПА применяются передовые технологии и методы, которые помогают детально оценить состояние пациента и подобрать наиболее адекватное лечение.
- Иммунологические тесты: позволяют выявлять антитела, связанные с этим заболеванием, такие как p-ANCA и c-ANCA, что способствует точной диагностики.
- Биопсия тканей: используется для получения образцов тканей, что помогает верифицировать наличие воспаления и поражения мелких сосудов.
- Магнитно-резонансная томография (МРТ): даёт возможность детально визуализировать внутренние органы и выявлять степень их поражения.
- Компьютерная томография (КТ): особенно полезна для оценки состояния лёгких и выявления патологий, связанных с МПА.
- Анализы крови и мочи: регулярный мониторинг этих показателей помогает оценивать активность болезни и эффективность проводимого лечения.
Схемы лечения
Терапия МПА направлена на подавление воспалительного процесса, устранение симптомов и предотвращение прогрессирования болезни. Современные методы лечения включают комбинацию медикаментозных и немедикаментозных подходов.
- Глюкокортикоиды: препараты, обладающие мощным противовоспалительным эффектом, являются основой терапии. Они помогают быстро снять острые проявления болезни.
- Цитостатики: лекарства, такие как циклофосфамид и метотрексат, применяются для подавления иммунной системы и уменьшения активности воспалительного процесса.
- Биологические препараты: современные моноклональные антитела, такие как ритуксимаб, воздействуют на конкретные клетки иммунной системы, уменьшая её патологическую активность.
- Плазмаферез: метод очистки крови от антител и токсинов, который может быть полезен в тяжёлых случаях.
- Иммуносупрессоры: препараты, которые помогают сдерживать агрессивные иммунные реакции, уменьшают риск обострений и поддерживают ремиссию.
Комбинирование различных методик и постоянная оценка их эффективности позволяют индивидуализировать терапию для каждого пациента. Это повышает шансы на длительную ремиссию и улучшение качества жизни больных микроскопическим полиангиитом.
Видео по теме:
Вопрос-ответ:
Что такое микроскопический полиангиит и каковы его основные симптомы?
Микроскопический полиангиит (МПА) – это редкое системное воспалительное заболевание, которое главным образом поражает мелкие кровеносные сосуды. Основные симптомы включают в себя быстро развивающуюся легочную и почечную недостаточность, слабость, потерю веса, лихорадку, и боли в мышцах и суставах. Симптомы могут варьироваться в зависимости от степени поражения различных органов и интенсивности воспалительного процесса.
Какие существуют методы диагностики микроскопического полиангиита?
Диагностика микроскопического полиангиита включает несколько этапов. Во-первых, врач собирает подробный анамнез пациента и проводит физическое обследование. Далее применяются лабораторные исследования, такие как анализ крови на показатели воспаления, исследование уровня автоантител и анализ мочи. Важную роль играют также визуализационные методы, такие как УЗИ почек и легких, а при необходимости биопсия пораженных тканей для подтверждения диагноза.
Каково лечение микроскопического полиангиита и его прогноз на будущее?
Лечение микроскопического полиангиита направлено на подавление воспалительного процесса и предупреждение повреждения органов. Оно включает использование иммунодепрессантов, таких как циклофосфамид или метотрексат, а также кортикостероидов для снижения воспаления. Современные биологические препараты, такие как ритуксимаб, также могут быть применены. Прогноз зависит от своевременности диагностики и качества лечения, однако при правильной терапии многие пациенты могут достичь ремиссии. Долговременный прогноз требует регулярного контроля и возможных коррекций лечения.
Есть ли какие-то меры профилактики микроскопического полиангиита?
В настоящее время специфических методов профилактики микроскопического полиангиита не существует, поскольку точные причины заболевания до конца не изучены. Образ жизни и генетическая предрасположенность могут играть роль, однако конкретные механизмы остаются неизвестными. Важно регулярно проходить медицинские осмотры и обращаться к врачу при появлении любых тревожных симптомов, чтобы своевременно начать лечение в случае необходимости.
Какую роль играет питание и образ жизни в лечении микроскопического полиангиита?
Хотя специфические диетические рекомендации для пациентов с микроскопическим полиангиитом отсутствуют, сбалансированное питание и здоровый образ жизни могут способствовать общему укреплению организма и поддержанию иммунной системы. Рекомендуется употребление продуктов, богатых антиоксидантами, витаминами и минеральными веществами. Избегание стрессов, регулярная физическая активность и отказ от вредных привычек также положительно влияют на общее состояние здоровья и могут способствовать лучшему самочувствию пациентов на фоне медикаментозного лечения.
Какие основные симптомы микроскопического полиангиита?
Основные симптомы микроскопического полиангиита включают в себя разнообразные проявления, которые могут различаться в зависимости от затронутых органов и систем. К ним можно отнести усталость, потерю аппетита, потерю веса, лихорадочные состояния, боли в суставах и мышцах, а также признаки поражения дыхательных путей, такие как кашель и одышка. Очень важно также обращать внимание на симптомы со стороны почек, такие как наличие крови в моче и повышение артериального давления, поскольку заболевание часто затрагивает почки.
Как проводится лечение микроскопического полиангиита?
Лечение микроскопического полиангиита потребует комплексного подхода и специфической терапии под наблюдением квалифицированного врача-специалиста. Основными целями лечения являются подавление воспалительного процесса и предотвращение прогрессирования заболевания. Первоначально используется интенсивная иммуносупрессивная терапия, включающая препараты, такие как циклофосфамид или ритуксимаб, совместно с кортикостероидами. После достижения ремиссии возможно постепенное снижение дозировки и переход на поддерживающую терапию с использованием менее агрессивных иммуномодуляторов. Важно также регулярно контролировать функцию почек и другие параметры, чтобы своевременно корректировать лечение и предотвращать возможные осложнения.